الجامعــة الوطنيــة الخاصــة
Al-Wataniya Private University
الواحة الأكاديمية للجامعة الوطنية الخاصة
ألزهايمر أم خرف؟ Alzheimer or Dementia ( أ.م.د. رغداء لحدو )
مسابقة أفضل مقالة علمية
مقالات كلية الصيدلة
الملخص
يُستخدم مصطلحا ألزهايمر Alzheimer، والخرف Dementia عادةً بالمعنى نفسه ولكن في الواقع لهما معنيان مختلفان. فالخرف ليس مرضًا محددًا، ولكنه مصطلح شامل يشير إلى وجود مجموعة من الامراض قد تؤدي الى الإصابة به. يؤثر الخرف عادة على قدرة المريض على أداء الأنشطة اليومية بنفسه، أحد مظاهره هو فقدان الذاكرة ولكن لا يعني فقدان الذاكرة لوحده الاصابة بالخرف. أما داء ألزهايمر فيُعد مرضًا دماغيًا محدد الاسباب والاعراض، ويتفاقم مع مرور الوقت نتيجة تغيرات غير ملحوظة في دماغ الشخص المصاب تشتد مع الزمن، حيث تظهر أعراض مثل فقدان الذاكرة ومشاكل اللغة وبمرور الوقت تتأثر قدرة الأفراد على أداء الأنشطة اليومية. عند هذه المرحلة، يُقال إن المريض مصاب بالخرف الناتج عن مرض ألزهايمر. أي أن ألزهايمر هو من أهم الأسباب المؤدية الى الخرف Dementiaولكنه ليس الوحيد. لم يتمّ إلى الآن التَّوصُّل إلى علاج فعال لمرض ألزهايمر، والعلاجات المُستخدَمة جميعها تساهم فقط في تخفيف حدّة الأعراض وإبطاء تطوُّر المرض.
الكلمات المفتاحية: مرض ألزهايمر، الخرف، بيتا أميلوييد، العلاج
- الخرف Dementia :
الخرف هو مصطلح يصف العديد من الاعراض الشائعة: ضعف في الذاكرة، ضعف مهارات التفكير والتقدير السليم للأمور، قلة التركيز والانتباه، تغيرات في مهارات اللغة، تغيرات في السلوك والقدرة على أداء الأنشطة اليومية. والخرف ليس مرضًا محددًا، إنما هناك العديد من الامراض التي قد تؤدي الى حدوثه وعليه يصنف الخرف الى العديد من الأنواع تبعا للمرض المسبب في حدوثه[1]، ويُعد داء ألزهايمر أكثر مسبب شيوعاً للخرف وسنأتي على شرحه لاحقاً.
أنواع الخرف تبعاً للمسببات [1]:
- خرف أجسام ليوي Lewy body dementia وخرف ألزهايمر Alzheimer’s disease وخرف بارنكسون Parkinson’s disease: يحدث نتيجة تجمع بروتينات محددة في الدماغ وهي الأنواع الأكثر شيوعاً.
- الخرف الوعائي Vascular dementia: يحدث نتيجة ضرر الاوعية الدموية التي تغذي الدماغ.
- الخرف الجبهي الصدغي Frontotemporal dementia: يحدث بفعل العديد من الأمراض التي تؤدي الى تلف الخلايا العصبية وفقدان التواصل بينها في القسم الجبهي الصدغي في الدماغ.
- الخرف المختلط Mixed dementia: يحدث نتيجة تجمع المسببات الانفة الذكر
- ألزهايمر Alzheimer:
مرض ألزهايمر Alzheimer’s disease، سُمِّي المرض باسم الطبيب النفسي والعصبي الألماني ألويس ألزهايمر الذي وصفه وشخَّصه في عام 1906 م [2] هو نوع من أمراض الدماغ، وهو مرض تنكسي، مما يعني أنه يصبح أسوأ مع مرور الوقت. يُعتقد أن مرض ألزهايمر يبدأ قبل ظهور الأعراض بحوالي 20 عاماً أو أكثر[3]، مع تغيرات طفيفة غير ملحوظة في دماغ الشخص المصاب، حيث تظهر أعراض مثل فقدان الذاكرة ومشاكل اللغة بعد سنوات من حدوث هذه التغيُّرات في الدماغ. تحدث الأعراض بسبب تلف الخلايا العصبية الواقعة في أجزاء الدماغ المشاركة في التفكير والتعلم والذاكرة (الوظيفة الإدراكية). يؤثر مرض ألزهايمر في جزء الدماغ المرتبط بالتعلم أولاً، لذا تشمل الأعراض المبكرة تغيرات في الذاكرة ومهارات التفكير والاستدلال العقلي. ومع تفاقم المرض، تزداد حدة الأعراض سوءًا وتشمل الاضطراب وتغيرات السلوك وبعض التحديات الأخرى.
يُصنف مرض ألزهايمر إلى نمطين[4]:
- مبكر الحدوث (Early-onset EOAD): يصيب الأشخاص بعمر 30-60 عاماً وهو نادر الحدوث حيث يُمثِّل 5% من مجموع مرضى ألزهايمر
- متأخّر الحدوث (Late-onset LOAD)،. تمثل معظم حالات مرض ألزهايمر، حيث تحدث الإصابة بهذا النمط بعد سن 60 عاماً.
2–1– مراحل مرض ألزهايمر Stages of Alzheimer’s Disease
هناك ثلاث مراحل لمرض ألزهايمر[5]:
- مرض ألزهايمر قبل السريري Preclinical Alzheimer’s Disease: في هذه المرحلة، التي لا تزال قيد التَّقصِّي، يعاني الأفراد من تغيُّرات قابلة للقياس(الواصمات الحيوية)، في الدماغ والسائل الدماغي الشَّوكي والدم، تُشير إلى العلامات الأولى لمرض ألزهايمر ، لكنهم لا يُظهرون في هذه المرحلة أعراضاً مثل فقدان الذاكرة. من المهم ملاحظة أنَّه ليس من الضرورة أن تتطوَّر حالة جميع الأفراد ذوي الواصمات الحيوية لمرض ألزهايمر إلى مرحلة MCI أو الخرف، على الرغم من أنَّ معظمهم يصل إلى هذه المراحل.
- ضعف الإدراك الخفيف (mild cognitive impairment MCI) بسبب مرض ألزهايمر: إنّ الأشخاص الذين يعانون من MCI بسبب مرض ألزهايمر لديهم واصمات حيوية تدلّ على وجود تغيّرات دماغيّة مرتبطة بمرض ألزهايمر ، كما يُبدي هؤلاء تراجعاً في الإدراك أكبر من المتوقع لسنِّهم، ولكن هذا التَّراجع لا يؤثِّر بشكل هام في الأنشطة اليومية. في MCI، ممكن ملاحظة التَّغيُّرات في القدرة على التَّفكير من قِبَل أفراد العائلة والأصدقاء، ولكن قد لا تكون ملحوظة للآخرين. إنّ ما يقارب (15–20)% من الناس في سنّ 65 عاماً أو أكبر يكون لديهم MCI لأسباب مختلفة. بيَّنت الدِّراسات أنّ 38% من الأفراد الذين يعانون من MCI طوّروا مرض ألزهايمر في غضون 5 سنوات من المتابعة.
- الخرف النَّاجم عن مرض ألزهايمرDementia Due to Alzheimer’s Disease: يتميّز الخرف الناجم عن مرض ألزهايمر بالأعراض الملحوظة المُتعلّقة بالذاكرة والتفكير والسلوك التي تُضعِف قدرة الشخص على العمل في حياته اليومية، جنباً إلى جنب مع ظهور تغيُّرات دماغية ومعالم حيوية تدل على وجود مرض ألزهايمر.
تختلف الوتيرة التي تتطوّر فيها أعراض الخرف من خفيفة إلى متوسطة إلى شديدة من شخص لآخر[6].
2–2-المعالم الحيوية المرتبطة بمرض ألزهايمرBiomarker associated with Alzheimer
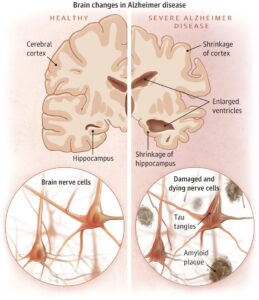
يظهر دماغ الشخص المصاب بألزهايمر وجود تراكم لقطع الببتيد بيتا أميلويد (تسمى لويحات بيتا أميلويد amyloid-beta plaques Aβ أو يطلق عليها لويحات الخرف Aβ Senile plaques) خارج الخلايا العصبية وتراكم شكل غير طبيعي من البروتين تاو (وتسمى عقد تاو tau tangles) داخل الخلايا العصبية وهما من أهم التغييرات الحاصلة في خلايا دماغ المصاب بمرض ألزهايمر (الشكل 1). تُساهم لويحات بيتا أميلويد في موت الخلايا عن طريق منع التواصل بين الخلايا العصبية على مستوى المشابك العصبية، في حين تمنع عقد التاو نقل المغذيات والجزيئات الأساسية الأخرى داخل الخلايا العصبية [7]. على الرغم من أنَّ العديد من الأفراد كبار السّنّ تتواجد لديهم بعض هذه اللويحات والتشابكات نتيجةً للشيخوخة، إلا أنَّ أدمغة المصابين بمرض ألزهايمر لديهم كمية أكبرٌ من هذه اللويحات والتشابكات في مناطق معينةٍ من الدماغ مثل الفصّ الصّدغي.
الشكل (1): مقارنة الخلايا العصبية بين دماغ سليم ودماغ مصاب بمرض ألزهايمر [8].
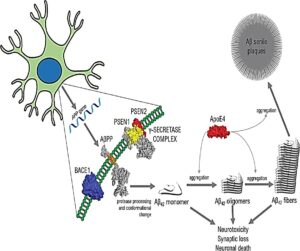
تكون الإصابات في حالات نادرة أشكالاً عائلية تتبع نمط الوراثة الجسمية (ليست مرتبطة بالجنس) السائدة، والتي تظهر قبل سن 65 عاماً [9]. يُسمى هذا الشكل من المرض باسم مرض ألزهايمر العائلي مُبكر البدء familial Alzheimer’s disease Early-onset. تُعزى معظم حالات ألزهايمر العائلي الجسمي السائد إلى طفراتٍ في واحدٍ من ثلاث جيناتٍ: التي تُشفِّر البروتين طليعة الأميلويد (APP)، والبريسنلين 1 والبريسنلين 2 (من عائلة الغاما سيكرتاز (γ-secretase [10]. تؤدّي معظم هذه الطَّفرات إلى زيادة إنتاج البيبتيد Aβ. أَشهر عامل اختطار وراثي مَعروف هو وراثة ألليل APOE ε4 (ألليل ε4 لصميم البروتين الشحمي E (APOE)). يُوجد بين 40-80% من مرضى ألزهايمر يحملون ألليل APOE ε4 واحداً على الأقل [11] (الشكل2).
الشكل (2): دور جينات الـ APP والبريسنلين 1 والبريسنلين 2 وAPOE 4 في تشكيل لويحات البيتا أميلويد [12].
2–3-عوامل اختطار الإصابة بخرف ألزهايمر Risk Factors for Alzheimer’s Dementia
باستثناء حالات مرض ألزهايمر المرتبطة بالطفرات الجينية والتَّثلُّث الصبغي 21، يعتقد الخبراء أنَّ مرض ألزهايمر، مثل الأمراض المزمنة الشائعة الأخرى، يتطوَّر نتيجة لعدَّة عوامل بدلاً من سبب واحد. نذكر منها: [6]
- تقدُّم السّن والتاريخ العائلي للإصابة بمرض ألزهايمر.
- مستوى التعليم: إنَّ الأشخاص الحاصلون على سنوات أكثر من التعليم هم أقل اختطاراً للإصابة بخرف ألزهايمر.
- نشاط الفرد الاجتماعي والعقلي طوال الحياة قد يدعم صحة الدماغ وربما يُقلِّل من اختطار خرف ألزهايمر والخرف بسبب أمراض أخرى.
- أذى الدِّماغ الرّضحي هو اضطراب في وظائف الدّماغ الطبيعية بسبب ضربة أو هزة في الرأس أو اختراق الجمجمة من قِبَل عنصر غريب).
- أمراض القلب والأوعية الدموية والعوامل المرتبطة بها تزيد من اختطار الإصابة بالخرف. تشمل هذه العوامل التَّدخين ومرض السكري، البدانة في منتصف العمر، ارتفاع ضغط الدم، وارتفاع الكوليستيرول في الدم.
2–4-علاج خرف ألزهايمر Treatment of Alzheimer’s Dementia
لا يوجد الى اليوم أي علاج دوائي متوفر للخرف الناتج عن ألزهايمر يوقف الضرر الحاصل للخلايا العصبية التي تسبب أعراض مرض ألزهايمر وتجعل المرض قاتلاً. العلاجات المُستخدَمة جميعها تساهم فقط في تخفيف حدّة الأعراض وإبطاء تطوُّر المرض، نذكر منها[6]:
- مثبطات الأستيل كولين استراز الانزيم الذي يستقلب الناقل العصبي الاستيل كولين، وافقت إدارة الغذاء والدواء الأمريكية FDA على ستة أدوية لعلاج مرض ألزهايمر: ريفاستيغمين، غالانتامين، دونيبيزيل، ميمانتين، جنباً إلى جنب مع دونيبيزيل، وتاكرين، تُحسِّن هذه الأدوية الأعراض بشكل مؤقّت عن طريق زيادة كمية النواقل العصبية في الدماغ.
- حاصرات مستقبل (NMDA) N-methyl-D-aspartate حيث يحصر الميمانتين مستقبلات NMDA في الدماغ ويقيها من التحفيز الزائد بواسطة حمض الغلوتاميك الذي يمكن أن يلحق الضرر بالخلايا العصبية.
- مضادات الذهان وهي مفيدة نوعاً ما في تخفيض العدوانية والذّهان لدى الأفراد المصابين بالألزهايمر، لكن لديها أعراض جانبية خطيرة مثل: السّكتة الدّماغية، الصعوبات في الحركة والتَّراجع الإدراكي.
- مضادات الالتهاب غير الستيرويدية Non-steroidal Anti-inflammatory Drugs NSAID)).
- خافضات الضغط (حاصرات مستقبلات الأنجيوتنسين Angiotensin II Receptor Blockers (ARBs)).
- العلاج غير الدوائي حيث يمكن للأفراد سليمي الإدراك استخدام علاجات غير دوائية بهدف إبطاء التراجع المعرفي أو منع الخرف، كاستخدام المُكمِّلات الغذائية، بما في ذلك فيتامينات مثلC، D، وE، أحماض أوميغا 3 الشحمية، والجنكوبيلوبا، التدريب المعرفي والنشاط البدني غير أن الدراسات أشارت إلى أن الأدلة لم تكن كافية لإثبات أن هذه العلاجات قد تحول دون التَّدهور المعرفي أو الخرف لدى كبار السن.
المراجع :
– Ward A, Tardiff S, Dye C, Arrighi HM Types of dementia. Alzheimer’s Association. https://www.alz.org/dementia/types-of-dementia.asp. Accessed Feb. 5, 2022.
– Plassman B.L, Langa K.M, Fisher G.G,et al. Prevalence of dementia in the united states: The aging, demographics,and memory study. Neuroepidemiology.2007; 29, 125–132.
– Gordon BA, Blazey TM, et al. Spatial patterns of neuroimaging biomarker change in individuals from families with autosomal dominant Alzheimer’s disease. Lancet Neurol 2018;17(3):241-50.
– Garg, S., & Roth, K. S. Alzheimer Disease and APOE-4. Retrieved from Medscape. 2015.
– Sperling RA, et al. Toward defining the preclinical stages of Alzheimer’s disease. Alzheimers Dement 2011;7(3):280-92.
– Gaugler J, James B, Johnson T, Marin A, Weuve JJA. 2019 Alzheimer’s disease facts and figures. Alzheimers Dement. 2019;15(3):321-387.
– National Institutes of Health. National Institute on Aging. What Happens to the Brain in Alzheimer’s Disease?. Accessed September 14, 2018.
– https://twitter.com/Rola_KF/status/1043046098166796288/photo/2
– Blennow K, de Leon MJ, Zetterberg H. Alzheimer’s disease. Lancet. 2006; 368 (9533): 387–403.
– Waring SC, Rosenberg RN. Genome-wide association studies in Alzheimer disease. Archives of Neurology. 2008; 65 (3): 329–34.
– Mahley RW, Weisgraber KH, Huang Y. Apolipoprotein E4: a causative factor and therapeutic target in neuropathology, including Alzheimer’s disease. Proceedings of the National Academy of Sciences of the United States of America. 2006; 103 (15): 5644–51.
– https://media.springernature.com/full/springerstatic/image/art
الجامعة الوطنية الخاصة
مواقع مرتبطة:
للتواصل :
- سوريا - محافظة حماة - الطريق الدولي حمص حماة
- 0096334589094
- 00963335033
- info@wpu.edu.sy
